Scientific journal
Scientific Review. Biological science
ISSN 2500-3399
ПИ №ФС77-57454
THE ANALYSIS OF THE EXPOSURE OF ANTHROPOGENIC FACTOR ON CHANGES IN THE CHEMICAL COMPOSITION OF ACHILLEA MILLEFOLIUM L. GROWING UNDER A VARIOUS ANTHROPOGENIC FACTOR BY BIOPHYSICAL METHODS OF OPTIC SPECTROSCOPY
В последнее время наблюдается повышенный интерес к лекарственным препаратам естественного происхождения. Поэтому востребованы исследования в области разработки новых методологий, направленных на определение фармакологически активных компонентов лекарственных растений, их эффективность и безопасность при использовании в фитотерапии и добавлении экстрактов в лекарственные препараты. Известно, что в растения загрязняющие вещества могут попадать вследствие адсорбции листьями или же в результате физиологического процесса почва – растения [1], потому сбор лекарственных растений необходимо проводить в местах с минимальной антропогенной (экологической) нагрузкой. Вследствие этого анализ состава растительного сырья является важным этапом диагностики при производстве лекарственных препаратов.
Одним из широко распространённых видов растений, обладающих ярко выраженным физиологическим действием на организм человека, является тысячелистник обыкновенный (Achillea millefolium L., семейство Asteraceae) – широко распространенный в северном полушарии вид, проявляющий устойчивость своего химического состава в зонах с антропогенным загрязнением [2, 3]. Однако устойчивость химического состава A. millefolium не исключает накопления в растении поллютантов, в зависимости от интенсивности антропогенной нагрузки. Тысячелистник обыкновенный является ценным лекарственным растением и представляет большой интерес в связи с широким спектром своих фармакологических свойств. Из литературных данных [4, 3] известно, что состав A. millefolium представляет собой комплекс из таких веществ, как флавоноиды, ахиллин, дубильные вещества, сложные эфиры, органические кислоты, полисахариды, витамины С и К и другие вещества. Основной же ожидаемый фармакологический эффект приходится на доминирующие в растении фенольные соединения [5]. Для медицинских целей используют отвары листьев и соцветий. Также тысячелистник входит в состав чаев и фитосборов (20–25 % от общего состава) [6].
Методы оптической спектроскопии позволяют быстро получать комплексную оценку исследуемого объекта с минимальным применением химических реагентов. Выбор биолюминесцентного метода для оценки токсичности обусловлен высокой скоростью получения результатов (в течение нескольких минут). Ранее была проведена работа по изучению влияния поллютантов на химический состав тысячелистника [7] методами оптической спектроскопии, в результате которой было установлено, что химический состав тысячелистника чувствителен к антропогенному загрязнению.
Цель работы состояла в проведении анализа наземных частей (соцветия и листья) A. millefolium, произрастающего в зонах с различной степенью антропогенной нагрузки с помощью методов оптической спектроскопии, позволяющих выявить корреляцию между параметрами химического состава фармакологических компонентов и степенью токсичности наземных частей растения.
Материалы и методы исследования
Объектом исследования служили надземные части (листья и соцветия) 11 популяций растений A. millefolium, из зон с различной степенью антропогенного воздействия в районе г. Красноярска [8]. Растения были собраны в период цветения – в июле 2015 г. В качестве контроля был выбран препарат фирмы ЗАО «Здоровье», производства 2015 г.
Для определения фенольных соединений и измерения токсичности были приготовлены водные экстракты соцветий и листьев из растений каждой исследуемой популяции по стандартной методике (ГОСТ 24027.2-80) [9].
Регистрация УФ-спектров водных экстрактов образцов проводилась с помощью спектрометра Cary Series UV-Vis-NIR Spectrophotometr (Agilent Technologies) в диапазоне 200–500 нм в кварцевых кюветах (с толщиной 1 мм). Концентрация определяемых веществ определялась по закону Бугера – Ламберта – Бера согласно которому, оптическая плотность D в УФ-спектрах изменяется в соответствии с концентрацией определяемых веществ:
D = εcl,
где ε – коэффициент экстинкции (л/моль/см), с – концентрация вещества (моль/л), l – толщина поглощающего слоя (см).
Измерение токсичности водных экстрактов производили при помощи комплекта реактивов аналитической биолюминесценции (КРАБ). Остаточное свечение биферментной сопряженной системы НАДН:ФМН – оксидоредуктаза-люцифераза измеряли в исследуемых экстрактах на биолюминометре 20/20n Single Tube Luminometer (GloMax). Реакцию биотестов определяют по величине остаточного свечения T = (I/ I0)*100 %, где I – интенсивность свечения в присутствии исследуемой пробы, I0 – контрольная интенсивность свечения и в соответствии с методикой, описанной в [10].
Регистрация ИК-спектров образцов осуществлялась согласно методике, описанной в [11] на Фурье-ИК-спектрометре Vertex 8 V (Bruker Optics). Навеска образца составляла 4 мг на 0,2 г KBr.
Результаты исследования и их обсуждение
Исследование состава Achillea millefolium с помощью УФ и ИК-спектроскопии
Спектры водных экстрактов образцов (рис. 1, А, Б) имеют выраженные максимумы на длинах волн λmax = 270–273 нм и λmax = 324–339 нм. Фенольные соединения являются доминирующими в изучаемом сырье и характеризуются наличием полос поглощения в диапазоне 260–350 нм [12, 7]. Для полученных спектров характерно смещение максимума поглощения в пределах 1–2 нм, что может быть связано с изменением содержания исследуемого вещества. Образец Am12, приобретённый в аптеке, представляет собой смесь из листьев, соцветий и стеблей тысячелистника обыкновенного. Потому для возможности сравнения собранных образцов и аптечного сырья была приготовлена эквивалентная смесь из образцов Am1-Am11 (рис. 1, В).
Среди полученных спектров наибольшей оптической плотностью характеризуется образец Am8 (популяция так же характеризуется относительно крупными размерами вегетативных органов и, возможно, относится к другому подвиду). Наименьшие значения содержания фенольных веществ в листьях установлены для образцов Am9 и Am10 (D меньше 0,38). Для остальных образцов значение оптической плотности (D = 0,92–0,63) варьируется в нешироких пределах. Так, максимальные значения D водных экстрактов соцветий характерны для образцов Am1, Am5, Am8 (D = 0,67–0,77). Минимальные – характерны для образцов Am9 и Am10 (D не превышает 0,45), произрастающих в зонах с повышенной антропогенной нагрузкой. Полученные данные согласуются с результатами работы [7]. Аптечный образец Am12 имеет значение D не более 0,58. Образцы Am9 и Am10 имеют наименьшие значения D, а значит, фармакологическое действие образцов из мкр-на Взлётка и деревни Плоское менее эффективно (фармакологическое действие образцов определялось по количеству фенольных соединений в исследуемом объекте по отношению к лекарственному сырью) относительно контроля.
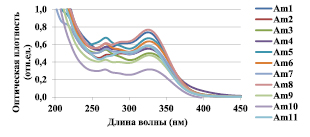
А
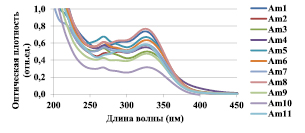
Б
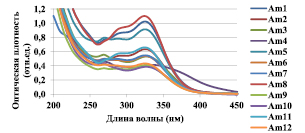
В
Рис. 1. УФ-спектры водных экстрактов наземных частей A. millefolium, А – листья, Б – соцветия, В – растение
Таблица 1
Исследование состава Achillea millefolium с помощью УФ-спектроскопии
|
№ популяции |
Дубильные вещества |
Хлорогеновая кислота |
|
Am1 |
1:1,58 |
1:1,61 |
|
Am2 |
1:0,84 |
1:0,68 |
|
Am3 |
1:1,10 |
1:0,84 |
|
Am4 |
1:0,92 |
1:0,64 |
|
Am5 |
1:1,61 |
1:1,44 |
|
Am6 |
1:1,00 |
1:0,85 |
|
Am7 |
1:1,01 |
1:0,86 |
|
Am8 |
1:1,54 |
1:1,73 |
|
Am9 |
1:0,73 |
1:0,65 |
|
Am10 |
1:0,86 |
1:0,61 |
|
Am11 |
1:0,98 |
1:1,04 |
|
Am12 |
1:1 |
1:1 |
Для анализа степени фармакологического действия образцов было составлено концентрационное соотношение дубильных веществ и хлорогеновой кислоты, содержащихся в исследуемых образцах к аптечному сырью, представленное в табл. 1. При отклонении значений более чем на 0,30 усл.ед. относительно контроля образцы были поделены на группы с более и менее эффективным фармакологическим эффектом относительно контроля.
График смеси из равных навесок соцветий, листьев и стеблей тысячелистника (рис. 1, В) имеет сходный вид с графиком поглощения листьев (рис. 1, А). В соответствии с этим было выдвинуто предположение, что основная фармакологическая ценность лекарственного сырья A. millefolium приходится на листья растения. Исключение составляют образцы с явным преобладанием значений D в водных экстрактах соцветий (Am1, Am5).
Для определения молекулярного строения компонентов лекарственного сырья использовалась регистрация ИК-спектров (рис. 2). Инфракрасный спектр биологического образца представляет собой суммарный спектр из перекрывающихся друг с другом полос поглощения различных функциональных групп органических веществ. При помощи литературных источников [13] в ИК-спектрах были обнаружены характерные для растительного объекта полосы на частотах 1109, 1161, 1256, 1320, 1378, 1513, 2854, 2925, 3370 см-1, что свидетельствует о колебаниях отдельных связей молекул целлюлозы, жиров, белков, углеводов, карбоксильных кислот, эфиров, фенолов, фуранов и фосфатных групп соответственно. Также во всех образцах обнаружены валентные колебания свободной и связанной ОН-группы (углеводы и аминокислоты) и внутри- и межмолекулярные Н-связи в димерах и полимерах (широкая полоса с максимумом 3440 см-1). Данная полоса также может включать в себя валентные колебания N-H-связей: первичные амиды 3540–3480 см-1, 3420–3380 см-1, вторичные амиды 3420–3460 см-1. Обнаружены валентные колебания С=О первичных, вторичных и третичных амидов (полоса около 1510 и 1651 см-1). Основные изменения в амплитуде ИК-спектров были установлены в диапазоне частот 500–2000 см-1.
Смещение валентных колебаний ОН- группы фенольных соединений (диапазон частот 3390–3500 см-1) обнаружено в ИК-спектрах образцов Am8 и Am10. Также были обнаружены деформационные колебания C-OH (1073 см-1) у образца Am10 и деформационные колебания О-Н и N-H групп (1620 см-1) для Am8, чем может быть обусловлено снижение фармакологического действия исследуемого образца. Установлено, что листья образцов Am8 и Am10 содержат в себе неорганические ионы MnO4- (840–850 см-1) и ацетиленовые соединения ртути (541 и 1603 см-1) [13], которые, согласно ГОСТ 937616, не должны содержаться в лекарственном сырье и, возможно, проникли в растение с дыханием.
Во всех образцах присутствуют колебания ионов PO43-, HPO42- (1100 см-1), нитросоединений и неорганического HCO3- (1320, 1400-1420 см-1). Вероятно, данные ионы были получены растениями из почвы через корневую систему.
Определение токсичности с помощью биолюминесцентного анализа
На рис. 3 представлены результаты оценки токсичности водных экстрактов образцов. Было установлено, что образец Am1 и водные экстракты листьев образцов Am5, Am7-10 классифицируются как токсичные (согласно методике, описанной в [10]) и не рекомендуются к использованию в качестве лекарственного сырья. Полученные экспериментально результаты совпадают с предположениями о степени загрязнённости исследуемых экстрактов растительного сырья на основе данных ИК-спектроскопии и [8].
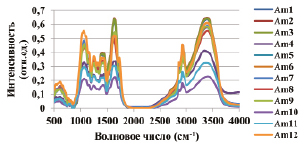
А
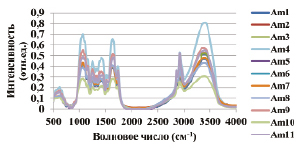
Б
Рис. 2. ИК-спектры наземных частей A. millefolium, А – листья, Б – соцветия
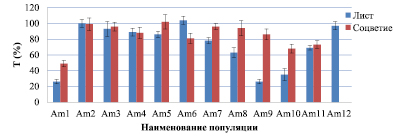
Рис. 3. Величина остаточного свечения измерялась при разведении образцов в 6 раз, чтобы избежать воздействия фоновой токсичности на КРАБ. Am 12 – контроль, относительно которого проводился анализ измерений. Значения остаточного свечения Т в пределах более 80–120 % соответствуют токсичным образцам [10]
Таблица 2
Сводная таблица
|
№ |
Место сбора (г. Красноярск) |
Антропогенная нагрузка |
Фармакологическая активность |
Биотестирование |
Обнаруженные отклонения состава от нормы |
Применение |
|
Am1 |
Окр. пос. Удачный, пойма р. Собачья речка |
умеренная |
высокая |
токсично |
– |
нет |
|
Am2 |
Мкр-н Академгородок |
умеренная |
умеренная |
нетоксично |
деформационные колебания ОН |
нет |
|
Am3 |
Берёзовая роща, зелёная зона, Октябрьский р-н |
низкая |
умеренная |
нетоксично |
– |
да |
|
Am4 |
Берег р. Енисей, ст. «Телефонисты», 10 км от г. |
низкая |
умеренная |
нетоксично |
– |
да |
|
Am5 |
Берег протоки р.Енисей, 9 км от г. |
низкая |
высокая |
умеренно |
деформационные колебания С-OH |
да |
|
Am6 |
Р-н. скалы Голубка, берег р. Енисей, 7 км от г. |
низкая |
умеренная |
нетоксично |
– |
да |
|
Am7 |
Посадки лесоинженерного факультета КГТУ, 5 км от г. |
низкая |
умеренная |
умеренно |
– |
да |
|
Am8 |
Село Зеледеево (Восточный Саян), 96 км от г. |
умеренная |
высокая |
токсично |
неорганические ионы MnO4-, соединения Hg, смещение валентных колебаний ОН |
нет |
|
Am9 |
Мкр-н Взлётка |
высокая |
низкая |
токсично |
соли аминов, соединения Hg |
нет |
|
Am 10 |
Деревня Плоское, Емельяновский р-н, 42 км от г. |
умеренная |
низкая |
токсично |
MnO4, соединения Hg, смещение валентных колебаний ОН |
нет |
|
Am 11 |
О. Татышев, зелёная зона |
низкая |
умеренная |
умеренно |
амид II, повышенное содержание PO4 |
да |
|
Am 12 |
Тысячелистника трава. ЗАО Фирма «Здоровье», 50 гр, Россия, 2015 г. |
низкая |
эталон |
эталон |
– |
да |
Согласно результатам по токсичности, в листьях накапливается больше поллютантов, что может быть связано с дыханием растения, а значит, листья более подвержены влиянию поллютантов по сравнению с соцветиями для одного и того же растения. Таким образом, очевидно, что образец Am1 произрастал в почве, загрязнённой продуктами антропогенного загрязнения. Имеет место предположение, что пониженное значение количества токсинов в соцветиях по сравнению с их содержанием в листьях связано с толерантностью биферментной системы к классам поллютантов, которые присутствуют в образце. Реакции тушения биолюминесценции (основным ферментом реакции которой является люцифераза) происходят посредством присутствия в лекарственном сырье полезных для организма антиоксидантов исключается, исходя из предположения, что биолюминесценция возникла как защитная реакция бактерий на кислород и имеет антиоксидантную природу [14, 15].
Заключение
Проведенный анализ качества сырья тысячелистника обыкновенного показал, что относительной безопасностью характеризуются образцы Am3 – Am7, собранные в лесных (берёзовая роща Академгородка) и луговых фитоценозах (на левобережье реки Енисей за пос. Удачный) в г. Красноярске и его окрестностях. Обнаруженные деформационные колебания ОН групп в образце Am2 (Академгородок), Am8 и Am10 (с. Зеледеево и Емельяново) говорят о невозможности применения данных образцов в фармакологичеких целях. Соединения ртути не должны присутствовать в образцах, а значит, образцы Am8-Am10 нельзя использовать как лекарственное сырьё. Образцы, собранные на о. Татышев, близ реки Енисей, не рекомендуется употреблять в больших количествах из-за повышенного содержания PO4.
В табл. 2 представлены данные, полученные в ходе исследования растительного объекта биофизическими методами.
В ходе проведённого исследования для наибольшего количества популяции обнаружена обратная зависимость биологической активности фармакологического состава (определяемой степенью содержания фенольных соединений в образцах) от интенсивности антропогенного воздействия. Все три используемых метода установили, что растения, произрастающие в зонах с высокой степенью антропогенной нагрузки, непригодны для использования в фармакологических целях, что важно учитывать при изготовлении фармакологических препаратов из данного сырья. Также установлено, что применение биолюминесцентных тест-объектов КРАБ применимо к определению токсичности в лекарственном сырье.
Авторы выражают благодарность Институту физики им. Л.В. Киренского СО РАН, Красноярск, за предоставление оборудования Vertex 8 V (Bruker Optics). За предоставление КРАБ авторы выражают благодарность кафедре биофизики ИФБиБТ Сибирского федерального университета, Красноярск.
Библиографическая ссылка
Слатинская О.В., Максимов Г.В. АНАЛИЗ ВОЗДЕЙСТВИЯ АНТРОПОГЕННОГО ФАКТОРА НА ИЗМЕНЕНИЕ ХИМИЧЕСКОГО СОСТАВА ТЫСЯЧЕЛИСТНИКА ОБЫКНОВЕННОГО (ACHILLEA MILLEFOLIUM L.) В ЗОНАХ С РАЗЛИЧНОЙ АНТРОПОГЕННОЙ НАГРУЗКОЙ БИОФИЗИЧЕСКИМИ МЕТОДАМИ ОПТИЧЕСКОЙ СПЕКТРОСКОПИИ // Научное обозрение. Биологические науки. 2017. № 4. С. 21-27;URL: https://science-biology.ru/en/article/view?id=1079 (дата обращения: 17.05.2026).


 science-review.ru
science-review.ru