Scientific journal
Scientific Review. Biological science
ISSN 2500-3399
ПИ №ФС77-57454
MOLECULAR GENETIC CHARACTERIZATION OF HLA-DRB GENE POLYMORPHISM IN THE SAMARKAND REGION POPULATION: FROM SEROLOGICAL ANTIGENS TO ALLELIC DIVERSITY
Введение
На сегодняшний день изучение иммунной системы и генов, участвующих в ее регуляции, а также функций, в которых они участвуют, является одной из актуальных проблем. Система HLA (Human Leukocyte Antigens – человеческие лейкоцитарные антигены) обладает высокой полиморфностью [1–3]. В настоящее время изучение этой системы в профиле различных народов и этнических групп необходимо для разработки HLA-профиля каждой популяции, что обеспечивает понимание регуляции иммунной системы и развитие показателей ее высокой или низкой активности. Сегодня актуально изучение особенностей иммуногенетического профиля, определяемого историческим развитием различных этнических групп и отношениями между популяциями. Знание «нормального» распределения HLA-генов и антигенов в отдельных популяциях важно для выявления связи HLA с заболеваниями, характерными для конкретных регионов, а также для понимания генетических основ патогенеза различных болезней [4, 5]. С другой стороны, данные о фенотипе и генотипе HLA популяции вместе с историческими, лингвистическими и другими исследованиями могут дать интересную информацию для определения происхождения различных этнических групп. Известно, что гены и антигены HLA участвуют в иммунных ответах, обеспечивая не только иммунный гомеостаз организма, но и взаимодействие иммунной системы с другими системами организма – нервной, эндокринной и другими, а также межклеточные взаимодействия во всех физиологических процессах [6, 7]. Изучение генов системы HLA и их аллелей на уровне конкретной популяции позволяет разработать маркеры на уровне HLA для этой популяции и предсказывать вероятность возникновения заболеваний [8, 9]. Исследование генов HLA класса I имеет большое значение при трансплантации органов для решения проблемы гистосовместимости, а эти данные широко применяются в клинической практике. Известно, что население Самаркандской области исторически характеризуется богатым этногенезом. Согласно историческим данным, формирование узбекского народа связано с участием двух крупных расовых элементов кавказского и монголоидного. Поэтому изучение HLA-профиля населения Самаркандской области является актуальной задачей. На сегодняшний день учеными широко применяется интеграционный подход к изучению системы HLA. Для этого создана международная биоинформационная база, в которую исследователи и ученые вносят первичную информацию о HLA-генах и белках [www.https://hla.alleles.org/nomenclature/index.html]. Поэтому изучение генетической структуры и этнических особенностей населения Самаркандской области имеет большое значение не только с исторической, но и с медицинской точки зрения. HLA-DRB1 относится к β-цепям генов HLA класса II. Молекулы II класса являются гетеродимерами, состоящими из α-цепи DRA и β-цепи DRB, обе из которых локализованы в мембране. HLA-DRB играет центральную роль в иммунной системе, представляя пептиды, полученные из клеток [10, 11] . Молекулы II класса экспрессируются в антиген-презентирующих клетках – B-лимфоцитах, дендритных клетках и макрофагах. β-цепь имеет молекулярную массу примерно 26–28 kDa и кодируется 6 экзонами, 1-й экзон кодирует сигнальный пептид, 2-й и 3-й экзоны кодируют два внешних домена, 4-й экзон кодирует трансмембранный домен, 5-й экзон кодирует цитоплазматический хвост [12–14].
Цель исследования – определить частоту встречаемости функциональных аллелей генов HLA-DRB у здорового населения Самаркандской области и оценить их популяционную структуру.
Материал и методы исследования
Молекулярно-генетические исследования проводились на базе отдела молекулярной генетики и цитогенетики Республиканского специализированного научно-практического медицинского центра гематологии Министерства здравоохранения Республики Узбекистан. Для исследования были отобраны образцы венозной крови 67 практических здоровых жителей Самарканда, не страдающих от серьезных хронических заболеваний. Формирование групп для молекулярно-генетических исследований проводилось методом случайного отбора. В качестве контрольной группы для проверки соответствия распределения генотипов равновесию Харди – Вайнберга использовалась вся совокупность обследованных здоровых индивидов (n = 67, n = 30 женщин, n = 37 мужчин) проживающих в Самаркандской области, представляющая однородную по этническому происхождению популяционную выборку. От всех участников было получено информированное согласие в соответствии с Хельсинкской декларацией. Средний возраст исследованных лиц составил 38,3±2,8 года. Ожидаемые частоты гомо- и гетерозигот рассчитывались на основании наблюдаемых аллельных частот HLA-DRB, что соответствует стандартному подходу в популяционно-генетических исследованиях. Полученные данные не выявили статистически значимых отклонений от равновесия Харди – Вайнберга, что указывает на относительную генетическую стабильность исследуемой популяции.
ДНК выделялась из крови с помощью колоночного метода QIAamp DNA Blood Mini Kit. Концентрация ДНК определялась флуориметрическим методом на приборе Qubit® 3.0. Генотипирование HLA-DRB проводилось методом ПЦР-SSP с использованием тест-систем, HLA-DRB1 и его аллелей HLA-DRB3 (Item number VHPS-4160), HLA-DRB4 (Item number VHPS-4161), HLA-DRB5 (Item number VHPS-4162), Biomol (Германия), ПЦР-условия: 10 мкл реакции, включающей 1 мкл ДНК, dNTP 0,2 мМ, Tris-HCl 67 мМ (pH 8,8), MgCl₂ 2,5 мМ, NaCl 50 мМ, 2-меркаптоэтанол 1 мМ, 1 ед. термостабильной ДНК-полимеразы.
Для анализа экспериментальных данных и проведения статистических расчетов в ходе исследования использовались специальные биостатистические модули программного комплекса Arlequin 3.5.2. Анализ проводился в соответствии со стандартами медицинской и генетической статистики, при этом применялись основные статистические показатели. В частности, в исследуемой группе определялись частоты аллелей, характерные для HLA-локусов.
Результаты исследования и их обсуждение
Частоты распространения аллелей HLA-DRB1 в узбекской популяции различаются среди этнических групп и популяций. Распределение аллелей DRB1 и его паралогов DRB3/4/5 и данные о частоте встречаемости полиморфизмов HLA-DRB в узбекской популяции Самарканда представлены в табл. 1.
В табл. 1 представлено популяционное распределение аллелей генов HLA-DRB, включающее количество выявленных аллелей, частоту их встречаемости (%) и аллельную (генную) частоту (X). Как видно из табл. 1, наибольшую распространенность имеют аллели DRB1*01:01, DRB1*03:01 и DRB1*04:01, частота встречаемости которых составляет соответственно 11,19; 10,45 и 9,70 %, что отражается и в высоких значениях аллельной частоты (0,112; 0,104; 0,097). Это указывает на их доминирующее положение в исследуемой популяции.
Таблица 1
Популяционное распределение аллелей генов HLA-DRB
|
HLA-DRB аллели |
Кол-во аллелей |
Частота встречаемости (%) |
Аллельная частота |
Частоты генов (Х) |
|
DRB1*0101 |
15 |
11,19 |
0,112 |
0,112 |
|
DRB1*01:02 |
11 |
8,21 |
0,082 |
0,082 |
|
DRB1*03:01 |
14 |
10,45 |
0,104 |
0,104 |
|
DRB1*04:01 |
13 |
9,70 |
0,097 |
0,097 |
|
DRB1*07:01 |
8 |
5,97 |
0,060 |
0,060 |
|
DRB1*08:01 |
3 |
2,24 |
0,022 |
0,022 |
|
DRB1*09:01 |
5 |
3,73 |
0,037 |
0,037 |
|
DRB1*11:01 |
3 |
2,24 |
0,022 |
0,022 |
|
DRB1*14:01 |
4 |
2,99 |
0,030 |
0,030 |
|
DRB1*15:01 |
3 |
2,24 |
0,022 |
0,022 |
|
DRB3*01:01 |
11 |
8,21 |
0,082 |
0,082 |
|
DRB3*01:02 |
4 |
2,99 |
0,030 |
0,030 |
|
DRB3*02:02 |
6 |
4,48 |
0,045 |
0,045 |
|
DRB4*01:01 |
9 |
6,72 |
0,067 |
0,067 |
|
DRB4*01:03 |
6 |
4,48 |
0,045 |
0,045 |
|
DRB5*01 |
8 |
5,97 |
0,060 |
0,060 |
|
DRB5*02 |
7 |
5,22 |
0,052 |
0,052 |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
Таблица 2
Ожидаемые гомо- и гетерозиготы аллелей HLA-DRB по закону Харди – Вайнберга
|
Аллель |
p (частота) |
p²-гомозиготы (%) |
2p(1-p)-гетерозиготы (%) |
|
DRB1*0101 |
0,112 |
1,25 |
19,84 |
|
DRB1*01:02 |
0,082 |
0,67 |
15,08 |
|
DRB1*03:01 |
0,104 |
1,08 |
18,64 |
|
DRB1*04:01 |
0,097 |
0,94 |
17,55 |
|
DRB1*07:01 |
0,060 |
0,36 |
11,28 |
|
DRB1*08:01 |
0,022 |
0,05 |
4,30 |
|
DRB1*09:01 |
0,037 |
0,14 |
7,13 |
|
DRB1*11:01 |
0,022 |
0,05 |
4,30 |
|
DRB1*14:01 |
0,030 |
0,09 |
5,82 |
|
DRB1*15:01 |
0,022 |
0,05 |
4,30 |
|
DRB3*01:01 |
0,082 |
0,67 |
15,08 |
|
DRB3*01:02 |
0,030 |
0,09 |
5,82 |
|
DRB3*02:02 |
0,045 |
0,20 |
8,55 |
|
DRB4*01:01 |
0,067 |
0,45 |
12,46 |
|
DRB4*01:03 |
0,045 |
0,20 |
8,55 |
|
DRB5*01 |
0,060 |
0,36 |
11,28 |
|
DRB5*02 |
0,052 |
0,27 |
9,88 |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
Аллели с умеренной частотой представлены вариантами DRB1*01:02, DRB3*01:01, DRB4*01:01 и DRB5*01, частота встречаемости которых колеблется от 5,97 до 8,21 %. Их вклад в генофонд популяции также является значимым, что подтверждается значениями генной частоты в пределах 0,060–0,082. Наименьшую распространенность, согласно табл. 1, демонстрируют аллели DRB1*08:01, DRB1*11:01, DRB1*15:01 и DRB3*01:02, частота встречаемости которых не превышает 3 %. Эти аллели относятся к редким вариантам в данной выборке.
В целом данные табл. 1 свидетельствуют о выраженной гетерогенности аллелей HLA-DRB и неравномерном распределении их частот в популяции, что может иметь значение для иммуногенетических и клинико-популяционных исследований.
Как показано в табл. 2, для аллелей генов HLA-DRB были рассчитаны ожидаемые значения гомо- и гетерозиготности в соответствии с законом Харди – Вайнберга на основе их аллельных частот (p). Полученные данные позволяют оценить степень генетического разнообразия и популяционную устойчивость исследуемой выборки. Для всех проанализированных аллелей характерны низкие ожидаемые значения гомозиготности (p²), что обусловлено умеренными и низкими аллельными частотами большинства вариантов. Наибольшие значения ожидаемой гомозиготности отмечены для наиболее распространенных аллелей локуса DRB1-DRB1*01:01 (1,25 %), DRB1*03:01 (1,08 %) и DRB1*04:01 (0,94 %), что согласуется с их доминирующим положением в популяции (табл. 2).
В то же время для редких аллелей, таких как DRB108:01, DRB111:01 и DRB1*15:01, ожидаемая гомозиготность минимальна и не превышает 0,05 %, что отражает их ограниченное распространение в исследуемой группе (табл. 2). Ожидаемая гетерозиготность (2p(1–p)) для всех аллелей значительно превышает показатели гомозиготности, что указывает на высокий уровень аллельного разнообразия. Наиболее высокие значения ожидаемой гетерозиготности характерны для аллелей DRB1*01:01 (19,84 %), DRB1*03:01 (18,64 %) и DRB1*04:01 (17,55 %), что подчеркивает их вклад в формирование гетерогенной иммуногенетической структуры популяции (табл. 2). Среди паралогичных генов DRB3, DRB4 и DRB5 также отмечается преобладание гетерозиготных состояний. Так, для аллелей DRB3*01:01, DRB4*01:01 и DRB5*01 значения ожидаемой гетерозиготности составляют 15,08; 12,46 и 11,28 % соответственно, что свидетельствует о сохранении функционального разнообразия комплекса HLA класса II (табл. 2).
Таблица 3
Общие популяционные показатели по локусу HLA-DRB
|
Показатель |
Значение |
|
Кол-во аллелей |
17 (функциональных) |
|
Средняя частота аллеля |
5,71 % |
|
Медиана |
4,47 % |
|
Минимальная частота |
1,49 % |
|
Максимальная частота |
22,30 % |
|
Стандартное отклонение (SD) |
2,96 % |
|
Коэффициент вариации (CV) |
51,8 % |
|
Ожидаемая гомозиготность (∑p²) |
6,77 % |
|
Ожидаемая гетерозиготность (H) |
93,2 % |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
Таблица 4
Сравнительное описание серологических и молекулярно-генетических исследований HLA-DR у населения Самарканда
|
Серологический HLA-DR антиген (1990-е) |
Частота (%) |
Молекулярные HLA-DRB аллели (современные) |
Частота аллеля (%) |
Примечание |
|
DR1 |
28,1 |
DRB1*0101 |
22,3 |
Основной аллель DR1 |
|
DRB1*01:02 |
8,95 |
Дополняющий аллель DR1 серологической группы |
||
|
DR7 |
37,8 |
DRB1*07:01 |
7,46 |
Подтверждено на молекулярном уровне |
|
DR9 |
23,2 |
DRB1*09:01 |
4,47 |
Соответствует DR9 антигену |
|
DR2 |
22,0 |
DRB1*15:01 |
4,47 |
Основной аллель DR2 серологической группы |
|
DR3 |
18,3 |
DRB1*03:01 |
5,97 |
Аллель подтвержден на молекулярном уровне |
|
DR4 |
13,4 |
DRB1*04:01 |
8,95 |
Серологические и молекулярные результаты совпадают |
|
DR11 |
15,9 |
DRB1*11:01 |
4,47 |
Подтверждено на уровне аллелей |
|
DR15 |
20,7 |
DRB1*15:01 |
4,47 |
Соответствует DR2/DR15 серологической группе |
|
– |
– |
DRB1*08:01 |
4,47 |
Не выявлено серологически |
|
– |
– |
DRB1*14:01 |
1,49 |
Редкий аллель |
|
– |
– |
DRB3*01:01 |
4,47 |
Не выявлено серологически |
|
– |
– |
DRB3*01:02 |
2,98 |
Дополнительный аллель DRB3 |
|
– |
– |
DRB3*02:02 |
2,98 |
Аллель DRB3 |
|
– |
– |
DRB4*01:01 |
4,47 |
Ген DRB4, отсутствует в серологии |
|
– |
– |
DRB4*01:03 |
2,98 |
Преимущество молекулярного типирования |
|
– |
– |
DRB5*01 |
1,49 |
Ген DRB5, только при генотипировании |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
В целом данные, представленные в табл. 4, указывают на низкий уровень ожидаемой гомозиготности и высокий уровень гетерозиготности для всех исследованных аллелей HLA-DRB. Это отражает выраженный полиморфизм локуса, соответствует равновесию Харди – Вайнберга и свидетельствует о генетической стабильности и высокой адаптивной способности популяции Самаркандской области.
Как представлено в табл. 3, локус HLA-DRB в популяции Самаркандской области характеризуется выраженным аллельным разнообразием и высоким уровнем генетической вариабельности. В исследуемой выборке идентифицировано 17 функциональных аллелей, что указывает на значительную полиморфность данного локуса (табл. 3).
Средняя частота аллелей составила 5,71 %, при медианном значении 4,47 %, что свидетельствует о преобладании в популяции средне- и низкочастотных вариантов. Минимальная частота аллеля достигала 1,49 %, тогда как максимальное значение составило 22,30 %, отражая выраженную неоднородность распределения аллелей в исследуемой группе (табл. 5). Уровень стандартного отклонения (SD = 2,96 %) и высокий коэффициент вариации (CV = 51,8 %) подтверждают значительную изменчивость аллельных частот и указывают на сложную структуру генофонда локуса HLA-DRB (табл. 3). Суммарная ожидаемая гомозиготность (∑p²) составила 6,77 %, тогда как ожидаемая гетерозиготность (H) достигла 93,2 %, что является характерным признаком высокополиморфных иммуногенетических локусов. Данные показатели свидетельствуют о преобладании гетерозиготных генотипов и высоком уровне генетического разнообразия, обеспечивающего адаптивную устойчивость популяции (табл. 3). Представленные в табл. 5 демонстрируют, что локус HLA-DRB в популяции Самаркандской области отличается генетической стабильностью, высокой гетерозиготностью и значительным адаптивным потенциалом, что важно для популяционных, иммуногенетических и клинических исследований.
Как показано в табл. 4, сравнение классических серологических исследований HLA-DR (1990-е гг.) [15] с современными молекулярно-генетическими данными HLA-DRB позволяет выявить соответствие и уточнить аллельное распределение в популяции. В целом молекулярный анализ подтвердил большинство ранее выявленных серологических антигенов и одновременно выявил дополнительное аллельное разнообразие, недоступное для серологического типирования (табл. 4). Для серологической группы DR1 частота антигена составляла 28,1 %, что соответствует аллелям DRB10101 (22,3 %) и DRB101:02 (8,95 %). Основной аллель DRB10101 определяет серологический тип DR1, тогда как DRB101:02 выступает как дополнительный вариант, ранее не различавшийся серологически (табл. 4). Антиген DR7 (37,8 %) на молекулярном уровне сопоставляется с аллелем DRB1*07:01 (7,46 %), что подтверждает точность серологического определения при ограниченной возможности различения редких аллелей. Аналогично серологический DR9 (23,2 %) соответствует молекулярному DRB109:01 (4,47 %), DR2/DR15- DRB1*15:01 (4,47 %) и DR3- DRB1*03:01 (5,97 %) (табл. 4).
Серологические группы DR4 и DR11 совпадают с молекулярными аллелями DRB104:01 (8,95 %) и DRB111:01 (4,47 %) соответственно, что подтверждает устойчивое соответствие классических антигенов и аллелей при современных методах типирования. Однако молекулярный подход выявил также ряд аллелей, которые ранее не обнаруживались серологически: DRB108:01, DRB114:01, DRB301:01, DRB301:02, DRB302:02, DRB401:01, DRB401:03 и DRB501, с частотой от 1,49 до 4,47 % (табл. 4). Это подчеркивает преимущество молекулярного типирования в выявлении редких и паралогичных аллелей, расширяющих понимание гаплотипического и аллельного разнообразия комплекса HLA класса II. Таким образом, табл. 4 демонстрирует, что молекулярно-генетические методы позволяют не только подтвердить результаты серологии, но и выявить дополнительное аллельное разнообразие, включая паралогичные гены DRB3, DRB4 и DRB5, что существенно повышает точность HLA-типирования и понимание иммуногенетической структуры популяции Самарканда.
На рисунке представлен анализ частот встречаемости основных аллелей HLA-DRB в исследуемой популяции, с разделением по полу. Каждый столбец отражает суммарное количество выявленных аллелей среди мужчин и женщин для соответствующего варианта гена. Анализ позволил определить распределение аллелей как среди мужской, так и среди женской части популяции, что является важным для оценки генетического разнообразия и выявления возможных половых различий в экспрессии иммуногенных локусов. На рисунке видно, что аллель DRB1*01:01 имеет наивысшую встречаемость в популяции, что соответствует его высокой частоте в общей выборке (табл. 1).
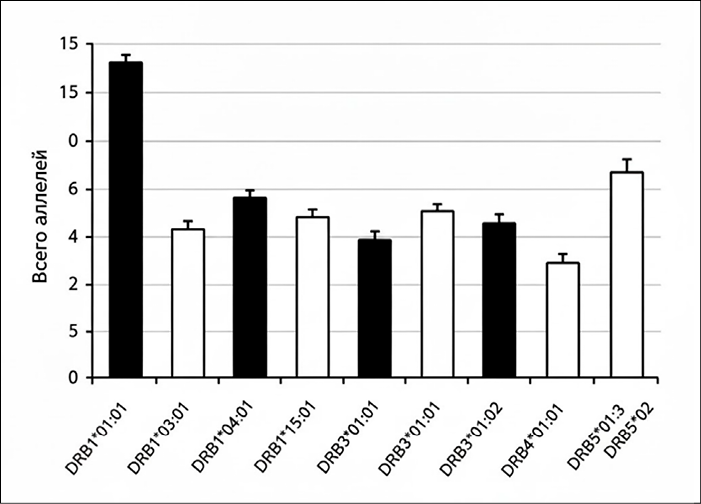
Распределение аллелей HLA-DRB по полу: черные столбцы – мужчины; белые столбцы – женщины Примечание: составлен авторами по результатам данного исследования
Таблица 5
Сравнительный анализ частот HLA-DRB1 с базой данных IMGT-HLA
|
Аллель |
Частота в Самарканде (%) |
Аллельная частота (f) |
Сравнительные популяции |
Вывод |
|
DRB1*01:01 |
11,2 |
0,112 |
Европа (Австрия, Бельгия, Дания, Чехия) 0,055–0,130; Центральная Азия (уйгуры, казахи) 0,018–0,065; Восточная Азия (китайцы) 0,004–0,026 |
Сходна с европейскими и центральноазиатскими популяциями, значительно выше, чем у восточноазиатских и африканских; отражает смешанное этногенетическое происхождение Самарканда |
|
DRB1*03:01 |
10,4 |
0,104 |
Европа 0,06–0,12; Центральная Азия (уйгуры, казахи) 0,03–0,14; Восточная Азия 0,005–0,02 |
Высокий европеоидный и центральноазиатский компонент, значительно выше, чем у восточноазиатских |
|
DRB1*04:01 |
9,70 |
0,097 |
Европа 0,06–0,12; Восточная и Центральная Азия низкие |
Умеренно низкая частота, влияние европейского компонента заметно |
|
DRB1*07:01 |
7,46 |
0,00449 |
Европа, Африка, Америка 0,10–0,26 |
Очень низкая частота; уникально для Самарканда; объясняется исторической изоляцией и миграцией |
|
DRB1*08:01 |
4,47 |
0,022 |
Европа 0,015–0,030; Восточная Азия (Китай) 0–0,005; Африка 0,001 |
Средняя европейская частота; значительно ниже в Восточной Азии и Африке |
|
DRB1*09:01 |
4,47 |
0,022 |
Европа 0,002–0,010; Восточная Азия (Китай) 0,135–0,283; Латинская Америка (кечуа, аймара) 0,087–0,333 |
Типичная для Европы и Центральной Азии, ниже, чем у Восточной Азии и Латинской Америки; отражает смешанное генетическое влияние региона |
Примечание: составлена авторами по источнику: URL: http://www.allelefrequencies.net (дата обращения: 01.02.2026)
Аллели DRB103:01 и DRB104:01 также демонстрируют высокую представленность, тогда как аллели DRB108:01, DRB111:01 и DRB4*01:01 встречаются реже. Паралогичные гены DRB301:01, DRB301:02 и DRB5*02 показывают умеренные значения, подтверждая их меньшую экспрессию по сравнению с DRB1. Разделение по полу позволило выявить, что распределение аллелей не демонстрирует выраженной гендерной предрасположенности, так как суммарные частоты между мужчинами и женщинами примерно равны для большинства аллелей. Это указывает на отсутствие полового диморфизма в распределении HLA-DRB в исследуемой популяции и подтверждает, что выявленные полиморфные аллели равномерно передаются и экспрессируются среди обоих полов.
Таблица 5 демонстрирует частоты аллелей HLA-DRB1 в популяции Самарканда с их сравнением с данными из других регионов мира, включая Европу, Центральную и Восточную Азию, а также Африку и Латинскую Америку. Анализ позволяет оценить этногенетические компоненты и уникальные особенности распределения аллелей в регионе. Аллель DRB1*01:01 встречается с частотой 11,2 % (f = 0,112), что сопоставимо с европейскими и центральноазиатскими популяциями [16, 17], однако значительно выше, чем у восточноазиатских и африканских групп. Это указывает на смешанное этногенетическое происхождение населения Самарканда и выраженный европеоидный компонент. Аллель DRB1*03:01 (10,4 %; f = 0,104) также демонстрирует сходство с европейскими и центральноазиатскими частотами и низкую встречаемость у восточноазиатских популяций, что подтверждает влияние европейского и центральноазиатского гаплотипического наследования.
Аллель DRB1*04:01 (9,7 %; f = 0,097) показывает умеренную частоту, что указывает на присутствие европейского компонента, однако его выраженность ниже, чем у DRB101:01 и DRB103:01. Аллель DRB1*07:01 характеризуется крайне низкой частотой (7,46 %; f = 0,00449) по сравнению с европейскими, африканскими и американскими популяциями, что может быть связано с исторической изоляцией, миграцией и локальной демографической историей Самарканда. Средне- и низкочастотные аллели, такие как DRB108:01 и DRB109:01, отражают смешанное влияние европейских, центральноазиатских и восточноазиатских компонентов. DRB108:01 присутствует на уровне европейских частот, тогда как DRB109:01, характерная для Восточной Азии и Латинской Америки, встречается в Самарканде на значительно более низком уровне, подчеркивая уникальность региональной популяции.
Заключение
В целом генетический профиль HLA-DRB1 населения Самарканда характеризуется высокой полиморфностью и смешанным этногенетическим происхождением, с доминированием европейских и центральноазиатских аллелей и наличием уникальных локальных вариаций, что имеет важное значение для популяционного анализа, иммуногенетических исследований и планирования донорских программ.
Conflict of interest
Библиографическая ссылка
Зиядуллаева Г. З., Душанова Г. А., Зиядуллаев Ш. Х., Рузыбакиева М. М. МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКАЯ ХАРАКТЕРИСТИКА ПОЛИМОРФИЗМА ГЕНОВ HLA-DRB В ПОПУЛЯЦИИ САМАРКАНДСКОЙ ОБЛАСТИ, ОТ СЕРОЛОГИЧЕСКИХ АНТИГЕНОВ К АЛЛЕЛЬНОМУ РАЗНООБРАЗИЮ // Научное обозрение. Биологические науки. 2026. № 1. С. 64-72;URL: https://science-biology.ru/en/article/view?id=1452 (дата обращения: 24.05.2026).
DOI: https://doi.org/10.17513/srbs.1452


 science-review.ru
science-review.ru