Членистоногие по количеству видов и распространённости могут считаться самой процветающей группой живых организмов, они обитают практически повсеместно и способны жить в экстремальных условиях. Протеиназы этих организмов являются необычными ферментами, заметно отличающимися по энзиматическим характеристикам от своих аналогов позвоночных и, особенно, млекопитающих. Многие ферменты членистоногих обладают уникальными свойствами и находят практическое применение в различных отраслях промышленности и медицине. Однако в настоящее время наиболее изучены психрофильные и психротолерантные ферменты из микроорганизмов [3,4].
Камчатский краб относится к отряду Decapoda, подотряду Anomura, семейству Lithodidae, подсемейству Uthodinae, роду Paralithodes. Этот краб – наиболее крупный из четырех промысловых видов северо-западной части Тихого океана. Обитание камчатского краба на родине приурочено к определенным водным массам – крабы совершают вертикальные миграции. По температурному режиму воды шельфа Берингова и Охотского морей в верхней части склона делятся на 3 слоя. Это поверхностный слой со значительными сезонными колебаниями – от высоких значений летом до отрицательных зимой, слой остаточного зимнего охлаждения с постоянно отрицательными значениями (-1,2°С) и промежуточный слой с постоянно низкой, но положительной температурой (около +1,5°С) У ракообразных (крабов, раков и креветок) гепатопанкреас является органом, совмещающим функции печени и поджелудочной железы. Из-за особенностей питания отряда Decapoda гепатопанкреас секретирует большое количество пищеварительных ферментов, гидролизующих все классы природных полимеров и обладающих широкой специфичностью и необычно высокой активностью. Ранее в нашей лаборатории было выделено и изучено несколько коллагеназ P. camtschaticus [5-7]. Цель этого исследования – изучение нового психротрофного катепсина from P. camtschaticus, определение его первичной структуры и энзиматических свойств. Цистеиновые лизосомальные катепсины, принадлежащие к С1 клану, по МЕROPS классификации, играют важную роль в метаболизме белка в клетке [8]. Катепсины декапод мало изучены [9], хотя они представляют несомненный интерес для фундаментальной энзимологии и прикладных исследований.
Выделение и очистка протеиназ камчатского краба
Трудности получения гомогенных эндопептидаз крабов связаны с тем, что в их гепатопанкреасе обнаруживается множество ферментов, лишь незначительно отличающихся молекулярной массой, изоэлектрической точкой, обладающих смешанной субстратной специфичностью. Ранее в нашей лаборатории был получен суммарный препарат протеиназ гепатопанкреаса камчатского краба «Морикраза», который применяется в составе мази для лечения ожогов, гнойно-трофических язв и послеоперационных рубцов.
В растворе Морикразы была обнаружена катепсиновая активность – гидролиз хромогенного субстрата Z-Ala-Phe-Arg-pNА [10] и частичное ингибирование этой активности при преинкубации препарата с раствором HgCl2. Активность по хромогенному субстрату усиливалась в присутствии цистеина и сохранялась при pH=5. Это дало основание полагать, что в Морикразе присутствует цистеиновая протеиназа катепсин. Для выделения фермента на первом этапе была проведена анионообменная хроматография на DEAE-Toyopearl в градиенте NaCl. После проведения ионообменной хроматографии, фракции, обладающие активностью по ZD-Ala-Phe-Arg-pNА и ингибирующиеся Hg2+, были собраны, сконцентрированы методом ультрафильтрации и нанесены на сефадексе G-50 fine. Пик, обладающий искомой активностью, был сконцентрирован методом ультрафильтрации и исследован методом SDS-электрофореза в ПААГ.
В итоге была достигнута степень очистки в 582 раза. Выход по активности составил 8,23%, однако результат может быть заниженным, так как многие протеиназы, содержащиеся в исходном материале, активны по субстрату ZD-Ala-Phe-Arg-pNА (в особенности мажорная сериновая протеиназа РС1 и трипсин).
Для того чтобы удостовериться в гомогенности полученной катепсиновой фракции, на SDS-электрофорез было нанесено избыточное количество белка (рис. 1). Видно, что присутствующая примесь незначительна, возможно это остаток неактивированного профермента.
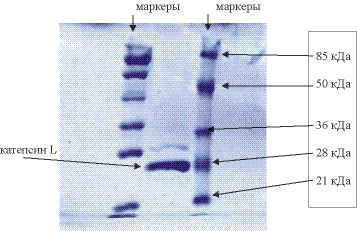
Рис. 1. Аминокислотная последовательность катепсина L из гепатопанкреаса of Red King Crab (P. camtschaticus)
Далее был получен и секвенирован полноразмерный ген катепсина L камчатского краба. Нуклеотидная последовательность была транслирована в аминокислотную последовательность профермента (рис. 2).

Рис. 2. SDS-PAGE катепсина L PC. Электрофорез образцов в 12% полиакриламидном геле, где: (1) полоса фракции очищенного фермента соответствуетo 28 kDa (катепсин L). Полоса, соответствующая 32 kDa, принадлежит проэнзиму. (2) стандарты (85-21 kDa, Fermentas SM-0441)
Анализ кДНК гена и транслированной аминокислотной последовательности показал, что профермент содержит 324 аминокислотных остатка, рассчитанная молекулярная масса 35,4 кДа; pI = 4,88.
Известно, что катепсины L как прокариот, так и эукариот, содержат высококонсервативную лидерную последовательность (16-18 аминокислотных остатков), за которой следует про-последовательность (60-100 аминокислотных остатков).
Лидерная последовательность состоит преимущественно из гидрофобных аминокислотных остатков, что облегчает транспорт катепсина по секреторному пути. Про-последовательность необходима для корректного фолдинга белка, временного нгибирования протеазной активности и транспорта неактивного профермента в эндосомы. В данном случае, аминокислотная последовательность начинается с метионина, который впоследствии отщепляется. Лидерная последовательность выражена слабо, скорее всего, она представлена 19 аминокислотными остатками и заканчивается на Thr19.Это наиболее вариабельный участок последовательности.
На основе сравнения с известными катепсинами других членистоногих было предположено место расщепления про-последовательности для получения зрелого фермента (обозначено красной стрелкой). Обычно, при созревании катепсина L у членистоногих, расщепление происходит вблизи участка высокой консервативности DWR. Более того, в участке P2` преимущественно находится Pro, реже – другая гидрофобная аминокислота (например, Ala). Зрелая форма исследуемого катепсина камчатского краба содержит предположительно 220 аминокислотных остатков, рассчитанная молекулярная масса составляет 23,78 кДа. Согласно SDS-электрофорезу в ПААГ молекулярная масса катепсина составляет 29 кДа, однако, следует учитывать, что на электрофорезе значения масс обычно бывают завышенными. Низкая изоэлектрическая точка, pI=4,82, является характерной чертой большинства ферментов членистоногих.
Для выявления особенностей в первичной структуре исследуемого катепсина, было выполнено сравнение его аминокислотной последовательности с аминокислотными последовательностями катепсинов других членистоногих (Рис. 3).

Рис. 3. MALDI-MS анализ
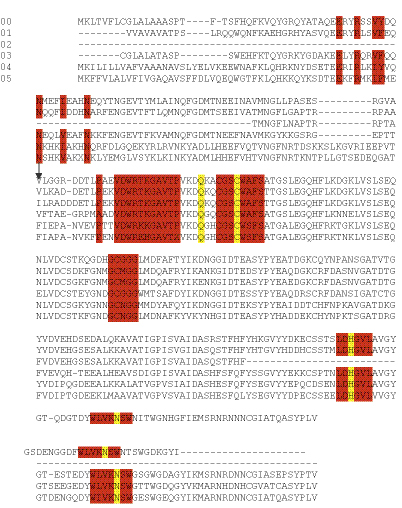
Рис. 4. Сравнение первичной структуры катепсинов L f из различных Decapoda. Высококонсервативный район отмечен красным, аминокислотные остатки, которые образуют активный центр - желтым, Cys образующий дисульфидные связи – in голубым. Сайт расщепления про-энзима указан стрелкой. 00 – катепсин L из Red King Crab (Paralithodes camtchatica); 01 – катепсин L из cathepsin L from Whiteleg Shrimp (Litopenaeus vannamei); 02 – катепсин L из cathepsin L from Giant Tiger Prawn (Penaeus monodon); 03 – катепсин L из катепсин L из cathepsin L from Norway lobster (Nephrops norvegicus); 04 – катепсин L из – катепсин L из cathepsin L from African mosquito (Сulex aegypti); 05 – катепсин L из cathepsin L from dermestid beetle (Dermestes frischii)
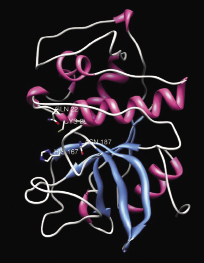
Рис. 5. Модель третичной структуры катепсина L РС. Розовым отмечены α-спирали, синим – β-слои, белым – петли. Активный центр в красном квадрате
Из приведенных данных видно, что исследуемый катепсин проявляет высокую степень сходства аминокислотной последовательности с катепсинами L других членистоногих (95-97% сходства). В целом, N-конец более вариабельный, C-конец более консервативный. Интересно, что С-концевые 5 аминокислотных остатка SYPLV присутствуют у подавляющего большинства представителей цистеиновых катепсинов членистоногих. Исследуемая аминокислотная последовательность содержит консервативный мотив GCNGG, характерный для большинства цистеиновых протеиназ. В нашем случае, Asn заменен на Gly. Это, вероятно, связано с психротрофностью фермента и увеличивает его лабильность. Катепсин L камчатского краба содержит мотив ERFNIN (EX3RX2(V/I)FX2NX3IX3N), характерный для всех представителей подсемейства катепсинов L. Однако Phe заменен на Tyr. Каталитический Cys окружен участком высокой консервативности. Шесть высококонсервативных остатков Cys, формирующих дисульфидные связи в папаине в позициях 22-65, 56-98, 157-207, присутствуют и в исследуемом катепсине. Общее низкое содержание Arg (4% от всех аминокислот) и отсутствие явных гидрофобных кластеров свидетельствует об адаптации катепсина L камчатского краба к работе при низких температурах (психротрофность). Третичная структура (рис. 5) представляет собой две цепи – тяжелая и легкая, связанные дисульфидными и водородными связями. Между цепями находится активный центр фермента и субстрат-связывающий участок. N-концевой домен образован 3 α-спиралями, С-концевой домен образован 1 α-спиралью и 4 β-листами. Такая организация вторичной структуры является типичной для цистеиновых катепсинов. Относительно большое количество петельных структур на поверхности белковой глобулы является характерной особенностью строения психротрофных ферментов. β-листы находятся, в основном, внутри глобулы и в районе субстрат-связывающего участка. На рис. 6 розовым цветом обозначены α-спиральные участки, синим – β-листы, белым – петли. Красным прямоугольником выделен активный центр фермента (аминокислотные остатки Gln22, Cys28, His167, Asn187). N-концевой домен образован тремя a-спиралями, С-концевой домен образован 1 a-спиралью и 4 β-листами. Такая организация вторичной структуры является типичной для цистеиновых катепсинов. Относительно большое количество петельных структур на поверхности белковой глобулы является характерной особенностью строения психротрофных ферментов. β-листы находятся, в основном, внутри глобулы и в районе субстрат-связывающего участка.
Методом MALDI-MS было показано 100% соответствие первичной структуры выделенного катепсина, определенной по кДНК.
Рис.6. MALDI-MS анализы
Цветом обозначены идентичные участки сравниваемых последовательностей. Гидролиз трипсином (90.9% идентичности): Гидролиз глутпмилэндопептидазой (81.4% идентичности):
Так как катепсины, в основном, являются лизосомальными ферментами, то обычно они активны при кислых рН. Так, для катепсина L из жука-кожееда рН оптимум составляет 4,5; для катепсина L из тихоокеанской белой креветки - 5; большинство катепсинов L млекопитающих обладают наибольшей активностью при pH = 5,5.
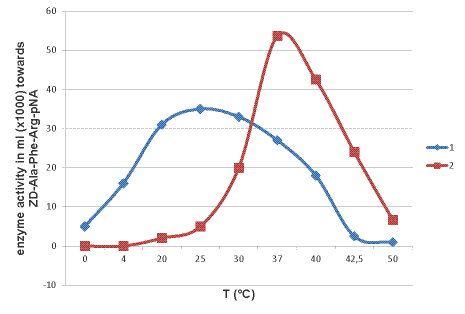
Рис. 6. Температурный оптимум. Активность фермента измерена по субстрату Z-Ala-Phe-Arg-pNA. 1 – катепсин L из краба P.camtschaticus; 2 – катепсин L из жука Dermestes frisii
Однако исследуемый катепсин камчатского краба показал наибольшую ферментативную активность по хромогенному субстрату ZD-Ala-Phe-Arg-pNА при слабощелочных условиях, с оптимумом рН = 8,0. При этом, катепсин L камчатского краба также сохраняет активность при кислых рН. Исходя из этих данных, можно предположить, что исследуемый катепсин является секретируемым белком, а не лизосомальным. Температурный оптимум катепсина камчатского краба находится при 25 ºC (рис.6). Однако, было обнаружено, что фермент способен гидролизовать хромогенный субстрат при температуре ниже 20 °С, и даже при 0 ºC. Это позволяет отнести исследуемый фермент к психротрофным. При повышении температуры до 50-60 ºC происходит резкое падение активности. Если провести 30-минутную пре-инкубацию фермента при 60 ºC и только потом добавить субстрат, то активность падает до 0. Это говорит о тепловой денатурации катепсина при данной температуре. Также в ходе работы было замечено, что исследуемый катепсин быстро теряет свою каталитическую активность при температуре выше 35 °С (падение удельной активности ~ на 25% за 4 часа нахождения при температуре 37 ºC).
Таблица 1
Выделение катепсина камчатского краба
|
этапы очистки |
количество белка (мг) |
Общая активность |
Активность в мл по ZD-Ala-Phe-Arg-pNa (мМ/мин•мл) |
Удельная активность в мл (мМ/мин•мг белка) |
Степень очистки |
|
исходный материал |
800 |
1312 |
262,4 |
1,6 |
1 |
|
DEAE-ToyoPearl |
5 |
97 |
64,6 |
19,4 |
12 |
|
G-50 fine |
0,116 |
108 |
39,3 |
931 |
582 |
Сравнение с катепсином L, жука выделенным из Dermestes frischii Т оптимум которого находится при 37°С, показало, что температурах меньше 10°С фермент жука не активен, при 42°С, в отличие от катепсина краба, сохраняет 24% активности.
Субстратная специфичность
Из таблицы 2 видно, что исследуемый катепсин обладает амидазной активностью и эффективно гидролизует синтетические хромогенные субстраты. С наибольшей эффективностью расщепляется синтетический субстрат ZD-Ala-Phe-Arg-pNА. № 2-6 являются стандартными субстратами для сериновых и трипсиноподобных протеиназ, как видно, некоторые из них (№ 2, 3) исследуемый катепсин хорошо гидролизует, другие (№ 4, 6) практически не гидролизует. Arg в положении Р1 является важным фактором гидролиза субстрата данным ферментом При сравнении активности катепсина по субстратам № 2 и 3, видно, что замена Arg на Lys в положении P1 уменьшает уровень гидролиза на 27%. Субстат трипсина (BZ-Arg-pNА) исследуемым катепсином практически не гидролизуется, несмотря на наличие Arg в положении Р1. № 13, 14 являются классическими субстратами папаина и бромелаина. Для исследуемого катепсина, по всей видимости, эти субстраты являются слишком короткими для эффективного связывания, поэтому их гидролиз идет на низком уровне. Нахождение Leu вместо Ala в положении Р1 в субстрате № 14 сильно снижает степень гидролиза. Также практически не гидролизуются субстраты эластаз (№ 18) и пролиновых эндопептидаз (№ 19).
Таблица 2
Действие катепсина L PC на синтетические субстраты. Все исследования были проведены при pH=8,0, 25 °C, в присутствии 5mM Cys
|
Cleavage site |
Organism |
Supposed/ proved |
|
104 R-DDTLPAEVDWRTK |
Paralithodes camtshaticus |
Proved on the basis of N-terminal sequence |
|
83-ТLPEKVDWTKG |
Litopenaeus vannamei |
Proved on the basis of N-terminal sequence11 |
|
106-MAADVDWRNK |
Pandalus borealis |
Proved on the basis of N-terminal sequence 12 |
|
121-KFPENVDWREH |
Dermestes frischii |
Suggested13 |
|
118-QLPGQIDWRDK |
Tenebrio molitor |
Proved on the basis of N-terminal sequence14 |
|
115-KLPAKVDWRQK |
Triatoma infestans |
suggested 15 |
|
120-KLPDTVDWRDK |
Sitophilus zeamais |
Suggested16 |
|
113-SWPWSKKVDWRSK |
Frankliniella occidentalis |
Suggested17 |
|
116-ADPNVQAVEEVDWRDS |
Diabrotica virgifera |
Proved on the basis of N-terminal sequence 18 |
|
123-VIPSKVDWREK |
Aphis gossypii |
suggested 19 |
|
126-TLAASIDWRTK |
Tetrahymena |
Proved on the basis of N-terminal sequence 20 |
Для изучения особенностей гидролиза пептидных связей был проведен гидролиз полученным катепсином физиологически активных пептидов известного строения – мелиттина, А и В цепей инсулина. Рис 7а.
Стрелками обозначены места гидролиза пептидов исследуемым катепсином. Красными стрелкам выделены места, наиболее предпочтительные для гидролиза.
Из приведенных данных видно, что исследуемый катепсин обладает широкой субстратной специфичностью. В положении Р1 предпочитает полярные, положительно заряженные аминокислотные остатки, особенно Arg. Чуть менее интенсивно идет гидролиз, если Arg в Р1 заменить на Lys. Однако, если в положении P1 находится His, то гидролиз не идет. Также, для активного гидролиза субстратов исследуемым катепсином важно, чтобы в положении Р2 находились гидрофобные аминокислотные остатки, что характерно для цистеиновых протеиназ. Предпочтительно, чтобы положение Р2 занимали Leu, Val, Ile Phe. Менее интенсивно катепсин расщепляет пептиды когда в положении P2 находится Trp или Аla. Удивительно, что в отличие от своих аналогов у других организмов (например, катепсины L из жука-кожееда и тихоокеанской белой креветки) исследуемый катепсин может гидролизовать субстраты с Asp в положении Р2. В нативных пептидных субстратах возможен гидролиз после полярных незаряженных аминокислотных остатков в положении Р1: Thr, Tyr, Ser. Также было установлено, что данный фермент не гидролизует небольшие пептиды. Это, скорее всего, связано с особенностями строения субстрат-связывающей впадины: из-за отсутствия “запирающей петли” исследуемый катепсин не проявляет экзопептидазную активность. Продолговатая форма субстрат-связывающей впадины, образованной, в основном, незаряженными аминокислотными остатками не способствует эффективному связыванию небольших пептидов.
Общая коллагенетическая активность исследуемого катепсина была проверена постепени гидролиза азоколлагена. Удельная активность по азоколлагену составляет 3,25 М/мин/мг белка. Далее был проведен гидролиз коллагена в течение 2 и 4 часов при комнатной температуре. Результаты приведены на SDS электрофорезе в ПААГ (рис. 7). Из приведенных данных видно, что исследуемый катепсин обладает коллагенолитической активностью. Коллаген X типа гидролизуется несколько быстрее, чем коллаген VI типа. В обоих случаях первые признаки гидролиза заметны уже через 2 часа инкубации фермента с коллагеном, причем в первую очередь расщеплению подвергаются β-цепи. После 4 часов инкубации катепсина с коллагеном VI типа a и β цепи полностью гидролизованы и коротких пептидов на электрофореграмме не видно. В случае коллагена X типа, за 4 часа происходит полный гидролиз всех трех видов цепей.
Таблица 3
Гидролиз синтетических хромогенных субстратов.
|
№ |
Субстрат |
активность в мл (мM/(мин · мл)) |
Удельная акт. (мМ/(мин · мг белка)) |
относительная акт. (в % относительно субстрата ZD-Ala-Phe-Arg-pNА) |
|
1 |
ZD-Ala-Phe-Arg-pNА |
39,3 |
802 |
100 |
|
2 |
Ac-Leu-Leu-Arg-pNА |
25,0 |
511 |
64 |
|
3 |
Ac-Leu-Leu-Lys-pNА |
18,6 |
380 |
47 |
|
4 |
D-Val-Leu-Lys-pNА |
0,2 |
5 |
1 |
|
5 |
ZD-Ala-Leu-Arg-pNА |
11,1 |
226 |
28 |
|
6 |
Gly-Arg-pNА |
2,3 |
46 |
6 |
|
7 |
BZ-Arg-pNА |
0,4 |
08 |
1 |
|
8 |
Glp-Ala-Ala-Leu-pNА |
4,0 |
82 |
10 |
|
9 |
ZD-Ala-Asp-Ala-pNА |
15,7 |
320 |
40 |
|
10 |
ZD-Ala-Glu-Ala-pNА |
2,6 |
54 |
7 |
|
11 |
ZD-Ala-Ala-Phe-pNА |
0,4 |
8 |
1 |
|
12 |
ZD-Gly-Gly-Leu-pNА |
0,0 |
1 |
0 |
|
13 |
Glp-Phe-Ala-pNА |
9,3 |
191 |
24 |
|
14 |
Glp-Phe-Leu-pNА |
0,8 |
17 |
2 |
|
15 |
ZD-Ala-Ala-Phe-Asp-pNА |
2,6 |
52 |
6 |
|
16 |
ZD-Ala-Ala-Met-Asp-pNА |
0,9 |
17 |
2 |
|
17 |
ZD-Glu-pNА |
0,2 |
5 |
1 |
|
18 |
Ac-Ala-Ala-Ala-pNА |
2,1 |
43 |
5 |
|
19 |
ZD-Ala-Ala-Pro-pNА |
0,3 |
5 |
1 |
Таблица 3
Действие ингибиторов на катепсин L РС. Активность определяли посинтетическому субстрату ZD-Ala-Ple-Arg-pNA. При t pH=8,0, 25 °C. Преинкубация 60 min
|
|
катепсин камчатского краба |
катепсин жука |
||||
|
T, °C |
4 |
23 |
37 |
4 |
23 |
37 |
|
Km, мМ |
0,043 |
0,033 |
0,16 |
0 |
0,12 |
0,050 |
|
rm, мМ/с |
4,9 |
0,13 |
0,74 |
0 |
0,98 |
0,68 |
|
kcat, 1/с |
26 |
0,69 |
3,9 |
0 |
5,2 |
3,6 |
|
kcat/Km, л/ммоль/с |
605 |
21 |
25 |
0 |
42 |
72 |
расчёт по методу Лайнувивера-Бёрка
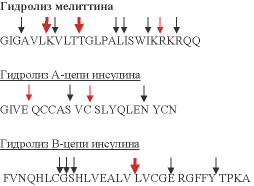
Рис. 7. Сайты расщепления природных пептидов катепсином L PC. Красные стрелки показывают главные позиции гидролиза, черными стрелками показаны отдельные сайты расщепления
Таблица 3. Сравнение кинетических параметров исследуемого катепсина с катепсином L из жука-кожееда по субстрату Z-Ala-Phe-Arg-pNА. Из приведенных в таблице 3 данных видно, что исследуемый катепсин из краба показывает относительно высокое сродство к синтетическому хромогенному субстрату Z-Ala-Phe-Arg-pNА. Эффективность катализа исследуемого катепсина при температурах выше +20ºС сравнима с таковой термофильного катепсина L из жука-кожееда. Заметные отличия наблюдаются при температуре +4 ºС: в то время как фермент из жука-кожееда не проявляет протеолитической активности, фермент из краба демонстрирует высокую эффективность катализа – на порядок выше, чем при температурах выше +20 ºС.
Ингибиторный анализ
Таблица 4
Действие ингибиторов на катепсин L камчатского краба
|
№ |
Ингибитор |
А410 |
Остаточная акт. (мM/мин·мл) |
% ингибирования |
|
1 |
HgCl2 |
0 |
0 |
100 |
|
2 |
E-64 |
0.049 |
0,99 |
82 |
|
6 |
Лейпептин |
0.056 |
1,1 |
80 |
|
3 |
Йодацетамид |
0,069 |
1,38 |
75 |
|
5 |
PMSF |
0.091 |
1,8 |
67 |
|
7 |
Соевый ингибитор трипсина |
0.231 |
4,6 |
16 |
|
8 |
Эндогенный ингибитор сериновых протеиназ из гепатопанкреаса камчатского краба |
0.216 |
4,3 |
21 |
|
Контроль |
0.275 |
5,5 |
Таблица .4 Действие ингибиторов на катепсин L камчатского краба Исследуемый фермент полностью ингибируется хлоридом ртути, специфическим ингибитором цистеиновых протеиназ. Катионы ртути могут конкурентно необратимо связываться с цистеином активного центра. 82% ингибирование исследуемой протеиназы E-64 и 80% ингибирование лейпептином лишний раз подтверждает принадлежность фермента к семейству папаиноподобных катепсинов. Чуть хуже на данный фермент действует йодацетамид – достигается 75% ингибирования активности. Соевый ингибитор трипсина практически не подавлял активность катепсина (16% ингибирование). Более того, эндогенный ингибитор сериновых протеиназ из гепатопанкреса камчатского краба снижал катепсиновуюактивность только на 21%. В целом, полученный профиль ингибирования является характерным для катепсинов L.
Таблица 5
|
Объект |
М (кДа) |
pI |
T oптимум (ºC) |
рН оптимум |
|
Камчатский краб (Paralithodes camtschatica) |
23,78 |
4,82 |
25 |
8,0 |
|
Тихоокеанская белая креветка (Litopenaeus vannamei1 |
31,5 |
4,63 |
- |
5,1 |
|
Северная креветка (Pandalus borealis) |
29 |
- |
40 |
6,0 |
|
Омар американский (Homarus americanus2 |
28 |
4,8 |
25 |
4,5 |
|
Клоп триатомовый (Triatoma infestans) |
23 |
4,7 |
37 |
5,5 |
|
Жук-кожеед (Dermestes frischii) |
24 |
4,7 |
40 |
4,5 |
|
Мучной хрущак (Tenebrio molito)r |
30 |
4,3 |
47 |
5,0 |
Таблица 5 Сравнение молекулярных и ферментативных свойств катепсинов L некоторых членистоногих.
В настоящее время сведения о катепсинах ракообразных очень скудные. Как видно из Таблицы 5, энзиматические свойства катепсинов L хорошо изучены не у всех видов членистоногих. В отличие от многих катепсинов L, катепсин камчатского краба обладает аномально щелочным оптимумом рН. Более того, заметен низкий температурный оптимум, идентичный температурному оптимуму катепсина L из американского омара, но гораздо ниже чем у обитающей в сходных температурных условиях северной креветки. рI и молекулярная масса исследуемого фермента лежат в стандартном диапазоне.
Таким образом, на основании проведенных исследований катепсин из гепатопанкреаса Red King Crab (Paralithosed camtschaticus) можно классифицировать как цистеиновую ротеиназу клана СА, семейства С1, субсемейства A. Фермент обладает психрофильными свойствами и может эффективно гидролизовать коллаген.
Библиографическая ссылка
Исаев В.А., Балашова M.В., Шагин Д., Шагина И., Еремеев H.Л., Руденская Г.Н. НОВЫЙ ПСИХРОФИЛЬНЫЙ КАТЕПСИН L ИЗ ГЕПАТОПАНКРЕАСА КРАСНОГО КОРОЛЕВСКОГО КРАБА (PARALITHODES CAMTSCHATICUS) // Научное обозрение. Биологические науки. 2016. № 6. С. 81-89;URL: https://science-biology.ru/ru/article/view?id=1028 (дата обращения: 16.05.2026).


 science-review.ru
science-review.ru