Введение
В настоящее время все засоленные земли в республике обеспечены дренажными канавами, общая протяженность которых составляет 120 тыс. км. Значение дренажных систем заключается в регулировании водно-солевого режима подземных минерализованных вод на сельскохозяйственных угодьях. Эффективность промывки почв от солей на таких участках резко возрастает, что способствует очищению земли от вредных соединений. Дренажные канавы делятся на два типа: естественные и искусственные. Естественные возникают в результате пересыхания русел рек и озер или вследствие геологических процессов. Искусственные создаются человеком и делятся на пять категорий: 1) открытые горизонтальные; 2) закрытые горизонтальные; 3) вертикальные; 4) смешанные; 5) вакуумные. Глубина залегания канавы напрямую зависит от уровня грунтовых вод: для достижения максимальной эффективности она должна располагаться ниже этого уровня [1; 2]. В течение вегетационного периода при орошении соли из глубоких слоев почвы поднимаются на поверхность, что повышает засоленность земель и снижает урожайность. Для предотвращения этого проводится промывка полей пресной водой, которая затем стекает в дренажные канавы. В отличие от ирригационных каналов, в дренажных системах в течение года сохраняется относительно стабильный режим течения, что создает особые условия для местной экосистемы [3]. Уровень минерализации воды в дренажных канавах Узбекистана колеблется в пределах 3–8 ‰ (промилле). Такая специфическая среда определяет условия обитания рыб. До настоящего времени ихтиологи преимущественно изучали видовое разнообразие рек и водохранилищ, в то время как исследования ихтиофауны дренажных канав Ферганской долины практически не проводились [4]. В связи с этим целью исследования стало изучение фауны и биоэкологических особенностей рыб в дренажных системах региона.
Материалы и методы исследования
Материалы для исследования собраны в дренажных канавах вертикального типа Ферганской долины в период с 2024 по 2025 г. Образцы отбирались с интервалом в 10–15 дней с мая по декабрь. Сбор материала осуществлялся с помощью ставных сетей (ячея 10×10 мм; 20×20 мм; 30×30 мм), рыболовных сачков и крючковой снасти. После анестезии рыб фиксировали в 10 %-ном растворе формальдегида, потом через 10 дней их переводили в 70 %-ный этанол. Дальнейшее обработка материала проводились по общепринятым методикам ихтиологии [5, с. 314–320]. Для определения биологических показателей (Правдин, 1966) проводили следующие измерения: длины тела рыбы без хвостового плавника (l); общая масса тела (Q); масса тела без внутренностей (q); а также определяли пол, стадии зрелости, возраст рыб, абсолютную и относительную плодовитость. Для определения возраста бралась чешуя. Определение возраста рыб производили по методике Правдина (1966) и Чугуновой (1959). Под индивидуальной абсолютной плодовитостью (ИАП) понимается число яиц, выметываемое самкой в данном нерестовом сезоне. Число ооцитов, отделившееся от общего фонда половой железы и вступившее на путь трофоплазматического роста, следует считать потенциальной сезонной плодовитостью. Для определения абсолютной плодовитости самок рыб из гонады отбиралась навеска массой 1 г, в которой производился полный подсчет количества икринок. Затем полученное число умножалось на общий вес гонады. Индивидуальная относительная плодовитость (ИОП) рассчитывалась как отношение абсолютной плодовитости к весу тела рыбы без учета внутренних органов.
Коэффициент зрелости (Кзр.) рыб определили по формуле
Кзр. = R*100 / Q,
где R – масса гонад, Q – общая масса тела рыб.
Гонадо-соматический индекс (ГСИ) определили по формуле
ГСИ = R × 100 / q,
где q – масса тела рыб без внутренностей [5, с. 107].
Таксономическая идентификация рыб проводилась с использованием определителей M. Kottelat, J. Freyhof. «Handbook of European freshwater fishes» [6], «Разнообразие рыб Узбекистана» И. М. Мирабдуллаева, А. Р. Кузметова, А. Р. Курбанова [7, c. 116] и «Рыбы Узбекистана» И. М. Мирабдуллаева [8, c. 220]. Статистическая обработка данных выполнялась с помощью программы MS Excel.
Зависимость «длина – масса» (LWR) рассчитывалась по уравнению
W = aLb,
где W – общая масса (г), L – общая длина тела (см), a – коэффициент пересечения; b – коэффициент регрессии. Коэффициенты a и b вычислены следующим линейным регрессионным логарифмом: log(W) = log(a)+b*log(L) [9, c. 140]. Все статистические вычисления произведены программой MS Excel 2019.
Результаты исследования и их обсуждение
Воспроизводительная способность рыб включает ключевые компоненты: половую зрелость, репродуктивный период и плодовитость, которые являются жизненно важными характеристиками для понимания жизненного цикла вида [10, c. 3–34]. Гонадо-соматический индекс (ГСИ) использовался в качестве индикатора репродуктивной активности [11, c. 88–89]. При отсутствии данных об икре и личинках ГСИ позволяет определить пиковые периоды нереста. Знание динамики развития гонад необходимо для управления популяциями [4]. Кроме того, внутри одного вида плодовитость может варьироваться в зависимости от адаптации к среде обитания [3; 12].
Установлено, что ихтиофауна дренажных канав Ферганской долины представлена 18 видами рыб относящимися к 5 отрядам и 10 семействам (табл. 1). Среди местных видов не зафиксированы рыбы, занесенные в Красную книгу Узбекистана. Пять видов имеют местное промысловое значение. Из выявленных видов 7 являются аборигенными, а 11 –интродуцированными. Основную часть фауны канав составляют мелкие виды, не имеющие промыслового значения.
Проанализирована динамика репродуктивных показателей серебряного карася (Carassius gibelio) с мая по декабрь (табл. 2). Данный вид размножается в весенне-летний период и относится к порционно нерестующимся рыбам [13]. Согласно табл. 2, именно в мае у самок наблюдается максимальная масса гонад и наиболее высокие показатели абсолютной и относительной плодовитости. В июне, несмотря на сохранение массы гонад на уровне мая, плодовитость снижается, что объясняется порционным выметом икры. С июля масса гонад и плодовитость резко падают, сигнализируя об окончании нерестового сезона. Начиная с ноября показатели потенциальной плодовитости начинают постепенно увеличиваться.
Таблица 1
Таксономический состав ихтиофауны дренажных канав Ферганской долины
|
Отряд |
Семейства |
Род |
Вид |
|
Cypriniformes Bleeker, 1859 |
Nemacheilidae Regan, 1911 |
Triplophysa Rendahl, 1933 |
Triplophysa strauchii (Kessler, 1874) |
|
Cyprinidae Rafinesque, 1815 |
Carassius Jarocki, 1822 |
Carassius gibelio (Bloch, 1782) |
|
|
Cyprinus Linnaeus, 1758 |
Cyprinus carpio Linnaeus, 1758 |
||
|
Schizothorax Heckel, 1838 |
Schizothorax eurystomus Kessler, 1872 |
||
|
Xenocyprididae Günther, 1868 |
Ctenopharyngodon Steindachner, 1866 |
Ctenopharyngodon idella (Valenciennes, 1844) |
|
|
Hemiculter Bleeker, 1860 |
Hemiculter leucisculus (Basilewsky, 1855) |
||
|
Hypophthalmichthys Bleeker, 1860 |
Hypophthalmichthys molitrix (Valenciennes, 1844) |
||
|
Acheilognathidae Bleeker, 1863 |
Rhodeus Agassiz, 1832 |
Rhodeus ocellatus (Kner, 1866) |
|
|
Gobionidae Bleeker, 1861 |
Abbottina Jordan & Fowler, 1903 |
Abbottina rivularis (Basilewsky, 1855) |
|
|
Gobio Cuvier, 1816 |
Gobio lepidolaemus Kessler, 1872 |
||
|
Pseudorasbora Bleeker, 1859 |
Pseudorasbora parva (Temminck & Schlegel, 1846) |
||
|
Leuciscidae Howes, 1991 |
Alburnus Rafinesque, 1820 |
Alburnus taeniatus Kessler, 1874 |
|
|
Leuciscus Cuvier, 1816 |
Leuciscus squaliusculus (Kessler, 1872) |
||
|
Rutilus Rafinesque, 1820 |
Rutilus lacustris (Pallas, 1814) |
||
|
Siluriformes Cuvier, 1817 |
Siluridae Cuvier, 1816 |
Silurus Linnaeus, 1758 |
Silurus glanis Linnaeus, 1758 |
|
Gobiiformes Günther, 1880 |
Gobiidae Cuvier, 1816 |
Rhinogobius Gill, 1859 |
Rhinogobius cf. lindbergi Berg, 1933 |
|
Anabantiformes Britz, 1995 |
Channidae Scopolli, 1777 |
Channa Scopoli, 1777 |
Channa argus (Cantor, 1842) |
|
Cyprinodontiformes Berg, 1940 |
Poeciliidae Bonaparte, 1831 |
Gambusia Poey, 1854 |
Gambusia holbrooki Girard, 1859 |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
Таблица 2
Особенности изменения репродуктивной способности у серебряного карася (Carassius gibelio) по месяцам в дренажных канавах
|
Пол |
Месяц |
n |
l, мм |
Q, г |
q, г |
Масса гонад, г |
ИАП (штук) |
ИОП (штук) |
Кзр. |
ГСИ |
|
Самка |
май |
12 |
149,2 ± 5,1 |
113,6 ± 8,2 |
78,9 ± 4,5 |
22,4 ± 2,1 |
26615 |
337 |
19,8 |
28,4 |
|
Самец |
май |
10 |
149,5 ± 4,8 |
106,4 ± 7,5 |
87,7 ± 5,1 |
1,5 ± 0,2 |
– |
– |
1,4 |
1,7 |
|
Самка |
июнь |
8 |
141,6 ± 6,2 |
108,7 ± 9,1 |
77,5 ± 3,8 |
18,1 ± 1,5 |
18610 |
240 |
16,6 |
23,5 |
|
Самец |
июнь |
11 |
139,2 ± 3,9 |
79,2 ± 6,4 |
65,5 ± 4,2 |
0,6 ± 0,1 |
– |
– |
0,75 |
0,9 |
|
Самка |
июль |
15 |
121,5 ± 4,4 |
62,3 ± 5,7 |
49,4 ± 3,1 |
3,8 ± 0,4 |
5827 |
118 |
6,1 |
7,7 |
|
Самец |
июль |
9 |
120,9 ± 5,3 |
59,8 ± 4,9 |
48,5 ± 2,8 |
0,5 ± 0,1 |
– |
– |
0,8 |
1,0 |
|
Самка |
август |
7 |
190,9 ± 10,2 |
102,9 ± 8,5 |
82,4 ± 6,4 |
6,7 ± 0,8 |
6110 |
74 |
6,5 |
8,1 |
|
Самец |
август |
6 |
131,7 ± 7,1 |
66,0 ± 5,2 |
55,2 ± 3,9 |
1,1 ± 0,2 |
– |
– |
1,6 |
2,0 |
|
Самка |
сентябрь |
10 |
121,1 ± 4,2 |
64,8 ± 5,1 |
53,1 ± 3,5 |
2,2 ± 0,3 |
3756 |
71 |
3,4 |
4,1 |
|
Самка |
октябрь |
14 |
112,3 ± 3,8 |
43,5 ± 4,2 |
38,9 ± 2,9 |
1,0 ± 0,1 |
3131 |
80 |
2,3 |
2,5 |
|
Самец |
октябрь |
12 |
110,9 ± 3,5 |
44,7 ± 3,8 |
40,6 ± 3,1 |
0,5 ± 0,1 |
– |
– |
1,0 |
1,1 |
|
Самка |
ноябрь |
9 |
115,0 ± 4,7 |
48,7 ± 4,5 |
42,0 ± 3,4 |
2,3 ± 0,4 |
6987 |
166 |
4,7 |
5,5 |
|
Самец |
ноябрь |
10 |
123,7 ± 5,2 |
59,3 ± 5,6 |
52,1 ± 4,0 |
1,1 ± 0,2 |
– |
– |
1,8 |
2,0 |
|
Самка |
декабрь |
8 |
105,9 ± 3,9 |
39,3 ± 3,1 |
31,8 ± 2,5 |
1,9 ± 0,3 |
6680 |
210 |
4,8 |
5,9 |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
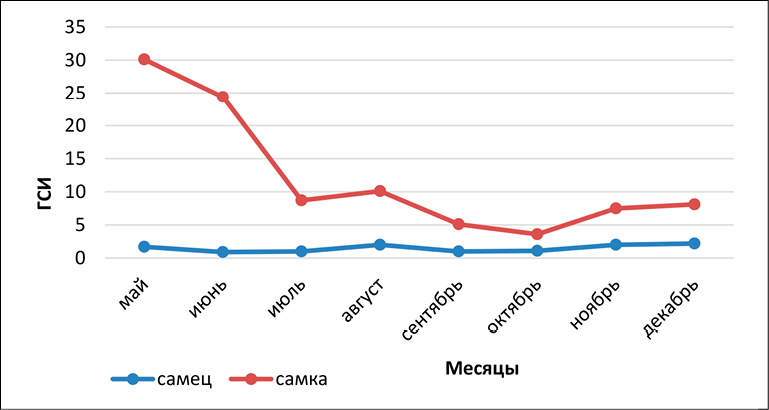
Рис. 1. Динамика развития гонадо-соматического индекса (ГСИ) по месяцам у самок и самцов Carassius gibelio Примечание: составлен авторами
Значения коэффициента b, близкие к 3,0, полученные для Carassius gibelio и Hemiculter leucisculus, указывают на изометрический характер роста, при котором масса тела увеличивается пропорционально длине. Следует подчеркнуть, что изометрия сама по себе не является прямым индикатором «благоприятных условий», однако в сочетании с гидрохимическими характеристиками среды она может отражать отсутствие выраженного физиологического стресса у рыб в данных водоемах.
Анализ гонадо-соматического индекса показал, что периоды созревания яйцеклеток и сперматозоидов у самок и самцов совпадают. У особей обоих полов значения индекса начинают расти в ноябре-декабре, достигая максимума в мае (рис. 1).
А) 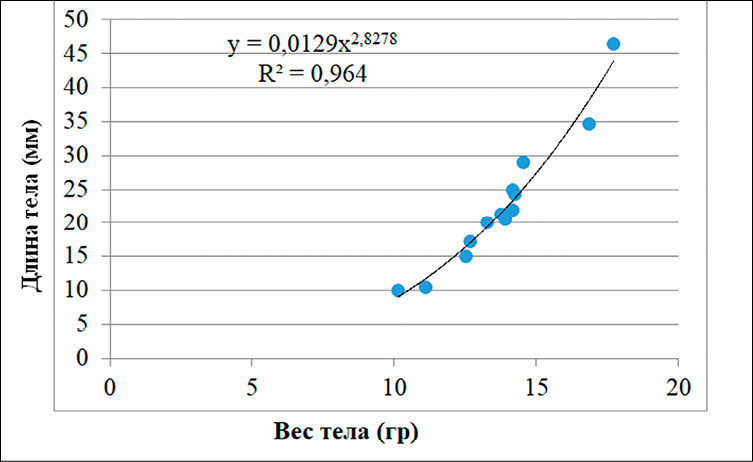
Б) 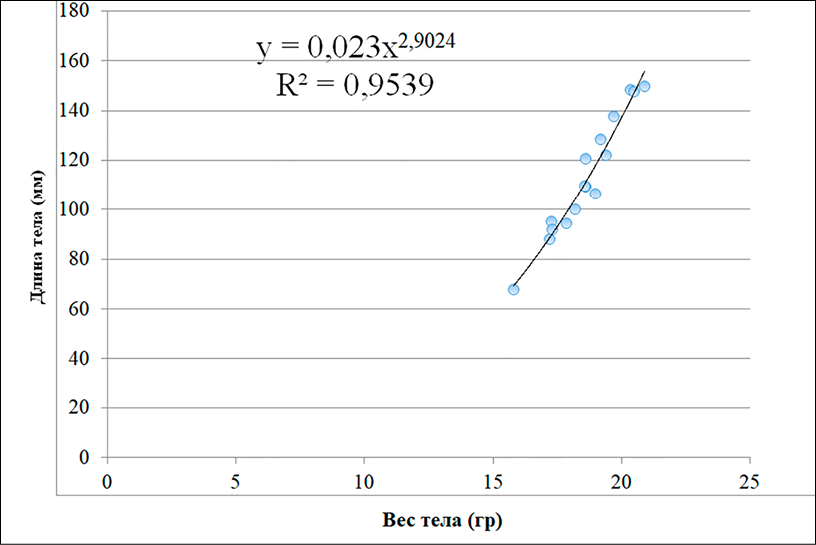
Рис. 2. Линейно-логарифмическое выражение связи длины и массы тела у Hemiculter leucisculus (А) и Carassius gibelio (Б) Примечание: составлен авторами
Взаимосвязь между линейным ростом и массой тела имеет важное диагностическое значение. Уравнение зависимости «длина – масса» (LWR) отражает экологическое состояние популяции в конкретном водоеме. Коэффициент b в норме находится в диапазоне 2,5–3,5. У Carassius gibelio и Hemiculter leucisculus, обитающих в дренажных канавах, этот показатель составил около 3,0, что характеризует изометрический рост (рис. 2). Полученные значения коэффициента b (≈ 3,0) для Carassius gibelio и Hemiculter leucisculus свидетельствуют об изометрическом росте, при котором масса тела увеличивается пропорционально длине. Это отражает стабильность формы тела рыб в условиях дренажных канав. Однако изометрический рост сам по себе не является доказательством благоприятных условий среды и должен интерпретироваться только в сочетании с гидрохимическими и физиологическими показателями [14; 15].
Заключение
Исследование показало, что ихтиофауна дренажных каналов Ферганской долины включает 18 видов (из 5 отрядов и 10 семейств), при этом значительную долю (61 %) составляют виды-интродуценты. Изучение репродуктивных особенностей Carassius gibelio подтвердило порционный характер икрометания с пиком активности в мае. Резкое снижение репродуктивных показателей, наблюдаемое с июля, указывает на завершение нерестового периода. Начало роста потенциальной плодовитости и ГСИ в ноябре свидетельствует о запуске очередного цикла гонадогенеза.
Выявленный изометрический рост (b ≈ 3,0) у Hemiculter leucisculus и Carassius gibelio свидетельствует о сбалансированном соотношении линейного роста и набора массы тела. В условиях специфической экосистемы дренажных канав это указывает на эффективную адаптацию данных популяций к гидрологическому режиму и текущей кормовой базе, что обеспечивает стабильное воспроизводство видов.
Библиографическая ссылка
Мамурова М.Х., Назаров М. Ш., Мирзахалилов М. М., Мукимов М. А. ФАУНА И БИОЭКОЛОГИЧЕСКИЕ ОСОБЕННОСТИ РЫБ ДРЕНАЖНЫХ КАНАВ ФЕРГАНСКОЙ ДОЛИНЫ // Научное обозрение. Биологические науки. 2026. № 2. ;URL: https://science-biology.ru/ru/article/view?id=1455 (дата обращения: 28.04.2026).
DOI: https://doi.org/10.17513/srbs.1455


 science-review.ru
science-review.ru